|
|
| (344 revisões intermediárias por 15 usuários não estão sendo mostradas) |
| Linha 1: |
Linha 1: |
| − | <span style="font-size:small;color:red">'''''Aos usuários do ceos, esclarecemos que foram revisados, atualizados e reescritos diversos medicamentos desde abril de 2016, dentre eles citamos os padronizados pelo Sistema Único de Saúde – SUS, pertencentes a Rename e os não padronizados, que foram incluídos de acordo com a necessidade. A data da atualização consta no final da página de cada medicamento, nutrição e procedimento. Portanto, salientamos que onde constam datas anteriores a abril de 2016, ainda não foram atualizadas.'''''</span>
| + | =='''Conhecendo a plataforma'''== |
| | | | |
| − | <span style="font-size:small;color:red">''Núcleo de Apoio Técnico – NAT/SC''</span>
| + | '''As informações sobre incorporações, padronizações, medicamentos, insumos e terapias disponíveis no SUS constam nesta plataforma de livre acesso.''' |
| | | | |
| − | =='''Medicamentos'''==
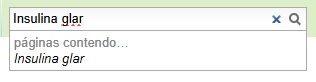
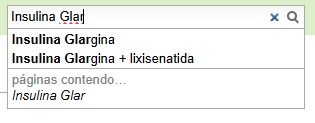
| + | Para melhor utilização, orienta-se que a busca deve ser feita com o nome exato do título da página (a busca diferencia letras maiúsculas de minúsculas). |
| | + | '''Exemplos:''' |
| | | | |
| − | <table border="3" cellpadding="6">
| + | [[Arquivo:Insulina_glargina_sem_correspondente.jpg]] |
| | | | |
| − | <tr><th><font size=4>[[A]]</font></th><th><font size=4>[[B]]</font></th><th><font size=4>[[C]]</font></th><th><font size=4>[[D]]</font></th><th><font size=4>[[E]]</font></th><th><font size=4>[[F]]</font></th><th><font size=4>[[G]]</font></th><th><font size=4>[[H]]</font></th><th><font size=4>[[I]]</font></th><th><font size=4>[[J]]</font></th><th><font size=4>[[K]]</font></th><th><font size=4>[[L]]</font></th><th><font size=4>[[M]]</font></th><th><font size=4>[[N]]</font></th><th><font size=4>[[O]]</font></th><th><font size=4>[[P]]</font></th><th><font size=4>[[Q]]</font></th><th><font size=4>[[R]]</font></th><th><font size=4>[[S]]</font></th><th><font size=4>[[T]]</font></th><th><font size=4>[[U]]</font></th><th><font size=4>[[V]]</font></th><th><font size=4>[[W]]</font></th><th><font size=4>[[X]]</font></th><th><font size=4>[[Y]]</font></th><th><font size=4>[[Z]]</font></th><th><font size=4>[[Todos]]</font></th></tr>
| + | [[Arquivo:Insulina_glargina_com_correspondente.jpg]] |
| | + | |
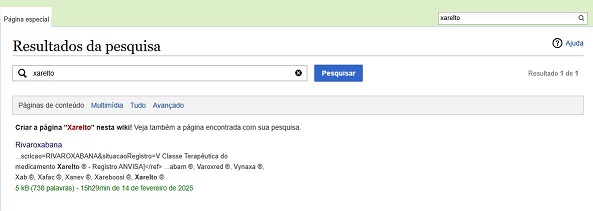
| | + | E caso a procura seja pelo nome comercial do medicamento/insumo, digitar o nome desejado e apertar tecla ENTER, sem esperar que apareça campo correspondente pela pesquisa. '''Exemplo:''' |
| | | | |
| − | </table>
| + | [[Arquivo:Busca_nome_comercial_2.jpg]] |
| | | | |
| − | =='''<span style="font-size:large;color:green"> Recomendações favoráveis sobre tecnologias avaliadas pela CONITEC</span>'''== | + | =='''Medicamentos'''== |
| | | | |
| − | *Certolizumabe pegol para o tratamento de artrite psoriásica em pacientes adultos com resposta inadequada a medicamentos modificadores do curso da doença - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Relatorios/Portaria/2017/PortariasSCTIE-54-60a62_2017.pdf Portaria nº 54, de 1° de dezembro de 2017]
| |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Recomendacao/Relat%C3%B3rio_levetiracetam_Epilepsia_290_FINAL_2017.pdf Levetiracetam para o tratamento da Epilepsia] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portaria_56_5_12_2017.pdf Portaria nº 56, de 1° de dezembro de 2017]
| + | <table border="3" cellpadding="10"> |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Recomendacao/RELATORIO_Naproxeno_Osteoartrite_Joelho_Quadril_Secretario_298_2017.pdf Ampliação de uso do naproxeno para osteoartrite de joelho e quadril] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_48-50-51-52-53.pdf Portaria nº 53, de 23 de novembro de 2017]
| + | <tr><th><font size=4>[[A]]</font></th><th><font size=4>[[B]]</font></th><th><font size=4>[[C]]</font></th><th><font size=4>[[D]]</font></th><th><font size=4>[[E]]</font></th><th><font size=4>[[F]]</font></th><th><font size=4>[[G]]</font></th><th><font size=4>[[H]]</font></th><th><font size=4>[[I]]</font></th><th><font size=4>[[J]]</font></th><th><font size=4>[[K]]</font></th><th><font size=4>[[L]]</font></th><th><font size=4>[[M]]</font></th><th><font size=4>[[N]]</font></th><th><font size=4>[[O]]</font></th><th><font size=4>[[P]]</font></th><th><font size=4>[[Q]]</font></th><th><font size=4>[[R]]</font></th><th><font size=4>[[S]]</font></th><th><font size=4>[[T]]</font></th><th><font size=4>[[U]]</font></th><th><font size=4>[[V]]</font></th><th><font size=4>[[W]]</font></th><th><font size=4>[[X]]</font></th><th><font size=4>[[Y]]</font></th><th><font size=4>[[Z]]</font></th> |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Recomendacao/Relatorio_memantina_Doenca-deAlzheimer_310_FINAL.pdf Memantina para doença de Alzheimer] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/PORTARIA_N_49_DE_9_DE_NOVEMBRO_DE_2017.pdf Portaria nº 49, de 8 de novembro de 2017]
| + | </table> |
| − | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relatorio_Fumarato_de_dimetila_Esclerose_Multipla_286_2017_FINAL.pdf Somatropina - Ampliação de concentrações para o tratamento de pacientes com síndrome de Turner e de pacientes com deficiência de hormônio de crescimento - Hipopituitarismo] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portaria_Somatropina.pdf Portaria nº 47, de 1º de novembro de 2017]
| |
| − | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relatorio_Fumarato_de_dimetila_Esclerose_Multipla_286_2017_FINAL.pdf Fumarato de dimetila no tratamento da esclerose múltipla remitente recorrente após falha com betainterferona ou glatirâmer] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 39, de 31 de agosto de 2017]
| |
| − | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relat%C3%B3rio_levetiracetam_convuls%C3%B5es_em_crian%C3%A7as_com_microcefalia_289_FINAL_2017.pdf Levetiracetam para o tratamento de convulsões em pacientes com microcefalia] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_33-39.pdf Portaria nº 38, de 31 de agosto de 2017]
| |
| − | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relatorio_laronidase_MPSI_FINAL_293_2017.pdf_Raltegravir_primeira_linha_HIV_FINAL_288_2017.pdf Laronidase como terapia de reposição enzimática na mucopolissacaridose tipo I] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 37, de 31 de agosto de 2017]
| |
| − | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/RELAT%C3%93RIO_Raltegravir_primeira_linha_HIV_FINAL_288_2017.pdf Raltegravir como opção terapêutica da primeira linha de tratamento das pessoas vivendo com HIV/Aids, mediante Protocolo Clínico e Diretrizes Terapêuticas] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 36, de 31 de agosto de 2017]
| |
| − | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relatorio_PCDT_Hepatite_C_Atualizacao_2017_Secretario_n275_2017.pdf Aprovar Protocolo Clínico e Diretrizes Terapêuticas de Hepatite C e Coinfecções, no âmbito do Sistema Único de Saúde - SUS] - '''Protocolo aprovado''' [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 33, de 31 de agosto de 2017]
| |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relat%C3%B3rio_Levetiracetam_Epilepsia_miocl%C3%B4nica_juvenil_282_2017.pdf Levetiracetam como terapia adjuvante em pacientes com epilepsia mioclônica juvenil resistentes à monoterapia] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 30, de 2 de agosto de 2017]
| + | =='''Medicamentos por CID e PCDT'''== |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relatorio_Trastuzumabe_CA_MamaMetastatico_CP.pdf Trastuzumabe para o tratamento do câncer de mama HER2-positivo metastático em primeira linha de tratamento] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 29, de 2 de agosto de 2017]
| + | '''Um novo recurso está disponível no site da CONITEC:''' o '''painel interativo de Medicamentos por CID e Protocolos Clínicos e Diretrizes Terapêuticas (PCDT)''' possibilita uma consulta rápida dos medicamentos e dos códigos da Classificação Internacional de Doenças (CID-10) contemplados nas diretrizes do Ministério da Saúde. |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Rasagilina_Parkinson_280_2017_FINAL.pdf Mesilato de rasagilina como terapia adjuvante à levodopa para o tratamento de pacientes com doença de Parkinson com complicações motoras] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 27, de 2 de agosto de 2017]
| + | '''Obs:''' ''a ferramenta não substitui a leitura integral do documento, uma vez que a indicação de cada medicamento exige atenção a critérios adicionais, como idade do paciente, histórico de tratamentos, estágio da doença, entre outros.'' |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Biotronik_Monitoramento_de_dispositivos_card%C3%ADacos_281_2017_FINAL_web.pdf Biotronik Home Monitoring System® para avaliação remota de pacientes portadores de Dispositivos Cardíacos Eletrônicos Implantáveis] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Legislacao/Portarias_SCTIE_26-27-29-30_Consulta_Publica_33-34-35-36.pdf Portaria nº 26, de 2 de agosto de 2017]
| + | <span style="color:blue">[https://www.gov.br/conitec/pt-br/protocolos-clinicos-e-diretrizes-terapeuticas/medicamentos-por-cid-e-pcdt '''Clique aqui'''] '''para acessar o painel.''' |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/Relatorio_Teriflunomida_EMRR_final.pdf Teriflunomida para primeira linha de tratamento da esclerose múltipla remitente recorrente] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Relatorios/Portaria/2017/PortariaSCTIE-17a19_2017.pdf Portaria nº 19, de 19 de abril de 2017]
| + | =='''Recomendações avaliadas pela CONITEC'''== |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2017/Relatorio_Tofacitinibe_AR__FINAL_241_2016.pdf Tofacitinibe para o tratamento de pacientes adultos com artrite reumatoide ativa moderada a grave] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Relatorios/Portaria/2017/PortariaSCTIE_08_2017.pdf Portaria nº 8, de 1º de fevereiro de 2017] | + | *[[Medicamentos incorporados - 2026]] |
| | | | |
| − | *[http://conitec.gov.br/images/Relatorios/2016/Relatorio_Rivastigmina_Alzheimer_final.pdf Rivastigmina via transdérmica (adesivo) para o tratamento de pacientes com demência leve e moderadamente grave do tipo Alzheimer] - '''Incorporar ao SUS''' - [http://conitec.gov.br/images/Relatorios/Portaria/2016/PortariasSCTIE_30a34_2016.pdf Portaria nº 31, de 20 de setembro de 2016] | + | *[[Medicamentos incorporados - 2025]] |
| | | | |
| | + | *[[Medicamentos incorporados - 2024]] |
| | | | |
| − | Segundo a [[CONITEC]], de acordo com a [http://www.planalto.gov.br/CCIVIL_03/_Ato2011-2014/2011/Lei/L12401.htm Lei n° 12.401 de 28 de abril de 2011] e o [https://www.planalto.gov.br/ccivil_03/_ato2011-2014/2011/decreto/d7646.htm Decreto n° 7.646 de 21 de dezembro de 2011 (art. nº 25)]: <span style="color:red">'''A partir da publicação da decisão de incorporar tecnologias em saúde, ou protocolo clínico e diretrizes terapêuticas, as áreas técnicas terão prazo máximo de 180 dias para efetivar a oferta ao SUS. Assim, o Ministério da Saúde tem um prazo de 180 dias para disponibilizar a tecnologia incorporada, a partir da data de sua publicação em DOU. Este prazo se faz necessário para os trâmites operacionais de negociação de preço, compra, distribuição e elaboração de protocolo clínico para orientação de uso racional.'''</span>
| + | *[[Medicamentos incorporados - 2023]] |
| | | | |
| − | =='''<span style="font-size:large;color:blue">Notícias</span>'''==
| + | *[[Medicamentos incorporados - 2022]] |
| | | | |
| − | '''1. [http://portalses.saude.sc.gov.br/index.php?option=com_docman&task=doc_download&gid=11917&Itemid=82 Desabastecimento dos Medicamentos Imunossupressores]
| + | *[[Medicamentos incorporados - 2021]] |
| | | | |
| − | Esclarecimento da Secretaria Estadual de Saúde de Santa Catarina referente aos medicamentos imunossupressores: Tacrolimo 1mg, Tacrolimo 5mg, Micofenolato Sódio 180mg, Micofenolato Sódico 360mg, indicados no tratamento de pacientes submetidos a transplantes.
| + | *[[Medicamentos incorporados - 2020]] |
| | | | |
| − | '''2. Portarias de Consolidação do SUS estão disponíveis para consulta online
| + | *[[Medicamentos incorporados - 2019]] |
| | | | |
| − | ''[http://portalms.saude.gov.br/noticias/agencia-saude/41940-portarias-de-consolidacao-do-sus-estao-disponiveis-para-consulta-online Novas portarias unificam normas de 1990 a 2017. Elas são o resultado de análise de 18.000 normas editadas pelo Gabinete do Ministro]''
| + | *[[Procedimentos, exames e insumos incorporados - 2026]] |
| | | | |
| − | As seis Portarias de Consolidação (PRC) editadas pelo Ministério da Saúde em outubro já estão disponíveis no site [http://portal2.saude.gov.br/saudelegis/LEG_NORMA_PESQ_CONSULTA.CFM Saúde Legis], que também pode ser acessado via o portal da Saúde. Elas sistematizam 749 portarias consideradas de conteúdo normativo e de efeitos permanentes ou duradouros. O trabalho é o resultado de análise de mais de 18 mil normas editadas pelo Gabinete do Ministro da Saúde nos últimos 27 anos.
| + | *[[Procedimentos, exames e insumos incorporados - 2025]] |
| | | | |
| − | As PRC estão divididas em seis eixos temáticos: direitos e deveres dos usuários da saúde, organização e funcionamento do SUS; políticas nacionais de saúde do SUS; redes do SUS; sistemas e os subsistemas do SUS; ações e serviços de saúde do SUS; e financiamento e transferência dos recursos federais para as ações e os serviços de saúde do SUS.
| + | *[[Procedimentos, exames e insumos incorporados - 2024]] |
| | | | |
| − | '''3. Brasil anuncia plano nacional para eliminação da hepatite C até 2030
| + | *[[Procedimentos, exames e insumos incorporados - 2023]] |
| | | | |
| − | ''[http://portalms.saude.gov.br/noticias/agencia-saude/41758-brasil-anuncia-plano-nacional-para-eliminacao-da-hepatite-c-ate-2030 Todos os pacientes diagnosticados passam a ter acesso ao tratamento, a partir de 2018, independente do grau de comprometimento do fígado]''
| + | *[[Procedimentos, exames e insumos incorporados - 2022]] |
| | | | |
| − | O Brasil anunciou o Plano Nacional para Eliminação da Hepatite C até 2030 com a oferta de tratamento para todos. A expectativa é tratar 657 mil pessoas nos próximos anos. A meta foi apresentada na quarta-feira (01/11/17) pelo ministro da Saúde, Ricardo Barros, durante a abertura da Cúpula Mundial de Hepatites 2017 – World Hepatitis Summit, em São Paulo (SP), que reúne ministros da Saúde, especialistas em saúde pública e ONGs para discutir a eliminação das hepatites virais em todo o mundo.
| + | *[[Procedimentos, exames e insumos incorporados - 2021]] |
| | | | |
| − | O protocolo atual considera elegíveis para tratamento no SUS os pacientes mais graves, nas fases 2, 3 e 4, os pacientes com coinfecção com HIV e pacientes com comorbidades, como doença renal crônica e manifestações extra-hepáticas. O Plano de Eliminação prevê que todos os pacientes diagnosticados com a doença serão atendidos, a partir de 2018, independente do grau de comprometimento do fígado.
| + | *[[Procedimentos, exames e insumos incorporados - 2020]] |
| | | | |
| | + | *[[Procedimentos, exames e insumos incorporados - 2019]] |
| | | | |
| − | '''4. Crianças com diabetes receberão no SUS o medicamento mais moderno | + | =='''Componentes da Assistência Farmacêutica'''== |
| | | | |
| − | ''[http://portalms.saude.gov.br/noticias/agencia-saude/30001-criancas-com-diabetes-receberao-no-sus-o-medicamento-mais-moderno O Ministério da Saúde está investindo R$ 135 milhões a mais para ofertar a insulina análoga, que melhorará a qualidade de vida desses pacientes]''
| + | *[[Componente Básico da Assistência Farmacêutica - CBAF]] |
| | | | |
| − | As crianças portadoras de diabetes tipo 1 terão à disposição no Sistema Único de Saúde (SUS) um dos mais modernos medicamentos para o tratamento da doença: a insulina análoga. Em alusão ao Dia das Crianças, comemorado no próximo dia 12, o Ministério da Saúde anunciou, nesta quarta-feira (11/10), que irá investir R$ 135 milhões, por ano, na compra do novo insumo. '''A expectativa é que o medicamento esteja disponível já em 2018.''' A nova aquisição será uma importante ferramenta na melhora da qualidade de vida de 100 mil crianças com maior dificuldade de controle da doença.
| + | *[[Componente Especializado da Assistência Farmacêutica - CEAF]] |
| | | | |
| | + | *[[Componente Estratégico da Assistência Farmacêutica - CESAF]] |
| | | | |
| − | '''5. Media Doctor - Avaliando a Qualidade de Notícias em Saúde
| + | *[[Tratamento oncológico no SUS|Componente da Assistência Farmacêutica em Oncologia - AF-Onco]] |
| − | | |
| − | Pesquisadores da Faculdade de Farmácia da UFMG lançam, no dia 14 de agosto, o primeiro portal acadêmico de avaliação de notícias em saúde no Brasil. O site faz parte do projeto MEDIA DOCTOR do Centro Colaborador do SUS - Avaliação de Tecnologias & Excelência em Saúde (CCATES) da Universidade Federal de Minas Gerais, em parceria com a Comissão Nacional de Incorporação de Tecnologias no SUS (CONITEC).
| |
| − | | |
| − | Preocupados com a qualidade da informação em saúde oferecida à população brasileira, os pesquisadores adotaram a metodologia Media Doctor, implantada em países como a Austrália, Estados Unidos, Canadá e Japão para analisar as notícias em saúde publicadas em jornais, revistas e portais online. O projeto é coordenado pelo professor Augusto Guerra, do Departamento de Farmácia Social, financiado pelo Ministério da Saúde, e traz no site (para acessar, [http://www.ccates.org.br/mediadoctor/ CLIQUE AQUI]) avaliações de reportagens sobre tecnologias em saúde. Para as avaliações, os pesquisadores examinam critérios científicos como indicação: benefícios; segurança; custo; alternativas; novidade tecnológica em saúde e independência da informação.
| |
| − | | |
| − | =='''<span style="font-size:large;color:black">Informações</span>'''==
| |
| − | | |
| − | - [[Acesso ao Componente Especializado da Assistência Farmacêutica - CEAF]]
| |
| − | | |
| − | - [[Agência Nacional de Saúde Suplementar (ANS)]] - <span style="font-size:large;color:red">''Novo!''</span>
| |
| − | | |
| − | - [[Antídotos]]
| |
| − | | |
| − | - [[Assistência Farmacêutica em Pediatria no Brasil]] - <span style="font-size:large;color:red">''Novo!''</span>
| |
| − | | |
| − | - [[Ausência de Registro na ANVISA]]
| |
| − | | |
| − | - [[Classificação Anatômica Terapêutica Química (ATC)]]
| |
| − | | |
| − | - [[Comissão de Farmácia e Terapêutica e Medicamentos de Uso Hospitalar]]
| |
| − | | |
| − | - [[Comissão Intergestores Bipartite CIB]]
| |
| − | | |
| − | - [[CONITEC]]
| |
| − | | |
| − | - [[Descontinuação de medicamentos - Anvisa]]
| |
| − | | |
| − | - [[Elenco de Medicamentos - CEAF]] - <span style="font-size:large;color:red">''Novo!''</span>
| |
| − | | |
| − | - [[Endereços/Contatos CACON/UNACONs]]
| |
| − | | |
| − | - [[Guia Entendendo a Incorporação de Tecnologias em Saúde no SUS – Como se Envolver]]
| |
| − | | |
| − | - [[Media Doctor - Centro Colaborador do SUS - Avaliação de Tecnologias & Excelência em Saúde (CCATES)]]
| |
| − | | |
| − | - [[Medicamentos - Conceitos e Informações Técnicas]]
| |
| − | | |
| − | - [[Medicamentos de Combate a AIDS e ao HIV - Antirretrovirais (ARV)]]
| |
| − | | |
| − | - [[Medicamentos Manipulados]]
| |
| − | | |
| − | - [[Medicamento "off label"]]
| |
| − | | |
| − | - [[Prescrições Médicas ]]
| |
| − | | |
| − | - [[Radiofármacos]]
| |
| − | | |
| − | - [[RENAME]]
| |
| − | | |
| − | - [[Tratamento oncológico no SUS]]
| |
| − | | |
| − | =='''<span style="font-size:large;color:black">Programas</span>'''==
| |
| − | | |
| − | - [[Componente Especializado da Assistência Farmacêutica (CEAF)]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF)]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Hanseníase]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Tabagismo]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Tracoma]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Tuberculose]]
| |
| − | | |
| − | - [[Programa Estadual de Vigilância e Controle das Hepatites Virais (PEHV)]]
| |
| − | | |
| − | - [[Programa Farmácia Popular do Brasil]]
| |
| − | | |
| − | =='''<span style="font-size:large;color:black">Links Úteis</span>'''==
| |
| − | | |
| − | - [http://bvsms.saude.gov.br/bvs/saudelegis/gm/2013/prt0874_16_05_2013.html Política Nacional para a Prevenção e Controle do Câncer]
| |
| − | | |
| − | - [http://cgj.tjsc.jus.br/saude/index.htm Portal Assistência à Saúde da Corregedoria-Geral da Justiça/SC]
| |
| − | | |
| − | - [http://rebrats.saude.gov.br/ Rede Brasileira de Avaliação de Tecnologias em Saúde - REBRATS]
| |
| − | | |
| − | - [http://www.ncbi.nlm.nih.gov/pubmed/ PubMed (artigos científicos da área da saúde)] | |
| − | | |
| − | - [http://www.scielo.br/?lng=pt SciELO (biblioteca eletrônica de periódicos científicos brasileiros)]
| |
| − | | |
| − | - [http://bvsalud.org/ Biblioteca Virtual em Saúde]
| |
| − | | |
| − | - [http://portal2.saude.gov.br/saudelegis/LEG_NORMA_PESQ_CONSULTA.CFM Saúde Legis]
| |
| | | | |
| | =='''Residual'''== | | =='''Residual'''== |
| | | | |
| − | - [[Alergia à proteína do leite de vaca]]
| + | *[[Doenças]] |
| − | | |
| − | - Artroplastia de quadril/[[Prótese (de quadril)]]
| |
| − | | |
| − | - [[Cross-linking]] (cirurgia para ceratocone)
| |
| − | | |
| − | - [[Curativos]]
| |
| − | | |
| − | - [[DMRI|Degeneração Macular Relacionada à Idade (DMRI)]]
| |
| − | | |
| − | - [[Eletroconvulsoterapia]]
| |
| − | | |
| − | - [[Internação Psiquiátrica Compulsória]]
| |
| − | | |
| − | - [[Intolerância à lactose]]
| |
| − | | |
| − | - [[Litíase urinária]] (pedras nos rins, ureteres ou bexiga)
| |
| − | | |
| − | - [[Meia Elástica]]
| |
| − | | |
| − | - [[Método Bobath]]
| |
| − | | |
| − | - [[Método Pediasuit]]
| |
| − | | |
| − | - [[Monitorização Neurofisiológica Intraoperatória]]
| |
| − | | |
| − | - [[Óculos]]
| |
| − | | |
| − | - [[Oxigenoterapia Domiciliar]]
| |
| − | | |
| − | - [[Oxigenoterapia Hiperbárica]]
| |
| − | | |
| − | - [[Pet-Scan]]
| |
| − | | |
| − | - [[Quimioterapia Intraperitoneal Hipertérmica]]
| |
| | | | |
| − | - [[Stent Farmacológico]]
| + | *[[Nutrição]] |
| | | | |
| − | - [[Videoartroscopia]]
| + | *[[Procedimentos Médicos Terapêuticos]] |
| | | | |
| − | ==Colaboradores de atualização - gestão NAT/SC==
| + | *[[Procedimentos Médicos Diagnósticos|Procedimentos Médicos Diagnósticos - Exames Complementares]] |
| | | | |
| − | Contribuíram para atualização do banco de dados CEOS (por meio de reuniões técnicas e envio de notas informativas sob responsabilidade de cada diretoria a respeito de seus respectivos programas):
| + | *[[Produtos para saúde (insumos)|Produtos para saúde - Insumos]] |
| | | | |
| − | - Diretoria de Assistência Farmacêutica (DIAF)
| + | *[[Terapias Complementares]] |
| | | | |
| − | - Diretoria de Vigilância Epidemiológica (DIVE)
| + | *[[Pedido de internação / asilamento]] |
| | | | |
| − | - Diretoria de Vigilância Sanitária Estadual (VISA)
| + | *[[Prontuário e Documentos Médicos]] |
| | | | |
| | + | *[[Prerrogativas Médicas]] |
| | | | |
| − | '''Responsáveis pelo conteúdo técnico anterior a março/2016: Comissão Multidisciplinar de Apoio Judicial - COMAJ'''
| + | *[[Tratamento Fora do Domicílio - TFD]] |
| | | | |
| | + | *[[Implante Dentário]] |
| | | | |
| − | Agradecimentos: Gerência de Tecnologia e Informação e Governança Eletrônica (GETIN)
| + | * [[Recomendações do COMESC]] |
Para melhor utilização, orienta-se que a busca deve ser feita com o nome exato do título da página (a busca diferencia letras maiúsculas de minúsculas).
Exemplos:
E caso a procura seja pelo nome comercial do medicamento/insumo, digitar o nome desejado e apertar tecla ENTER, sem esperar que apareça campo correspondente pela pesquisa. Exemplo: