|
|
| (618 revisões intermediárias por 15 usuários não estão sendo mostradas) |
| Linha 1: |
Linha 1: |
| − | ==Medicamentos== | + | =='''Conhecendo a plataforma'''== |
| − | Índice (páginas já concluídas)
| |
| | | | |
| − | <table border="3" cellpadding="6">
| + | '''As informações sobre incorporações, padronizações, medicamentos, insumos e terapias disponíveis no SUS constam nesta plataforma de livre acesso.''' |
| − | <tr><th><font size=4>[[A]]</font></th><th><font size=4>[[B]]</font></th><th><font size=4>[[C]]</font></th><th><font size=4>[[D]]</font></th><th><font size=4>[[E]]</font></th><th><font size=4>[[F]]</font></th><th><font size=4>[[G]]</font></th><th><font size=4>[[H]]</font></th><th><font size=4>[[I]]</font></th><th><font size=4>[[J]]</font></th><th><font size=4>[[K]]</font></th><th><font size=4>[[L]]</font></th><th><font size=4>[[M]]</font></th><th><font size=4>[[N]]</font></th><th><font size=4>[[O]]</font></th><th><font size=4>[[P]]</font></th><th><font size=4>[[Q]]</font></th><th><font size=4>[[R]]</font></th><th><font size=4>[[S]]</font></th><th><font size=4>[[T]]</font></th><th><font size=4>[[U]]</font></th><th><font size=4>[[V]]</font></th><th><font size=4>[[W]]</font></th><th><font size=4>[[X]]</font></th><th><font size=4>[[Y]]</font></th><th><font size=4>[[Z]]</font></th><th><font size=4>[[Todos]]</font></th></tr>
| |
| | | | |
| − | </table>
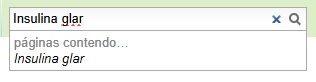
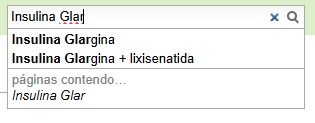
| + | Para melhor utilização, orienta-se que a busca deve ser feita com o nome exato do título da página (a busca diferencia letras maiúsculas de minúsculas). |
| | + | '''Exemplos:''' |
| | | | |
| | + | [[Arquivo:Insulina_glargina_sem_correspondente.jpg]] |
| | | | |
| − | =='''<span style="font-size:large;color:blue">''CONSULTAS PÚBLICAS E ENQUETES''</span>'''==
| + | [[Arquivo:Insulina_glargina_com_correspondente.jpg]] |
| | + | |
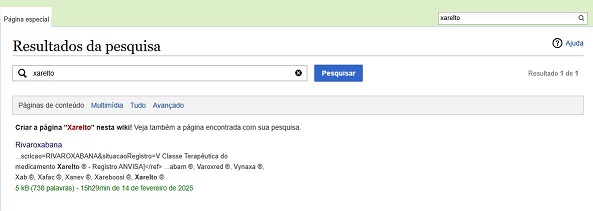
| | + | E caso a procura seja pelo nome comercial do medicamento/insumo, digitar o nome desejado e apertar tecla ENTER, sem esperar que apareça campo correspondente pela pesquisa. '''Exemplo:''' |
| | | | |
| | + | [[Arquivo:Busca_nome_comercial_2.jpg]] |
| | | | |
| − | * Foi publicado no Diário Oficial da União em 24 de outubro de 2016 a '''Consulta Pública nº 34''', de 21 de outubro de 2016 a respeito da recomendação da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde relativa à proposta de incorporação no SUS dos '''bevacizumabe para o tratamento do câncer de colo de útero metastático, persistente ou recorrente.''' Fica estabelecido o prazo de 20 (vinte) dias, a contar da data de publicação desta Consulta Pública, para que sejam apresentadas contribuições devidamente fundamentadas.
| + | =='''Medicamentos'''== |
| | | | |
| | | | |
| − | * Foi publicado no Diário Oficial da União em 14 de outubro de 2016 a '''Consulta Pública nº 31''', de 11 de outubro de 2016 a respeito da recomendação da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde relativa à proposta de incorporação no SUS dos '''medicamentos tópicos para o tratamento da Otite Externa Aguda'''. Fica estabelecido o prazo de 20 (vinte) dias, a contar da data de publicação desta Consulta Pública, para que sejam apresentadas contribuições devidamente fundamentadas.
| + | <table border="3" cellpadding="10"> |
| | | | |
| | + | <tr><th><font size=4>[[A]]</font></th><th><font size=4>[[B]]</font></th><th><font size=4>[[C]]</font></th><th><font size=4>[[D]]</font></th><th><font size=4>[[E]]</font></th><th><font size=4>[[F]]</font></th><th><font size=4>[[G]]</font></th><th><font size=4>[[H]]</font></th><th><font size=4>[[I]]</font></th><th><font size=4>[[J]]</font></th><th><font size=4>[[K]]</font></th><th><font size=4>[[L]]</font></th><th><font size=4>[[M]]</font></th><th><font size=4>[[N]]</font></th><th><font size=4>[[O]]</font></th><th><font size=4>[[P]]</font></th><th><font size=4>[[Q]]</font></th><th><font size=4>[[R]]</font></th><th><font size=4>[[S]]</font></th><th><font size=4>[[T]]</font></th><th><font size=4>[[U]]</font></th><th><font size=4>[[V]]</font></th><th><font size=4>[[W]]</font></th><th><font size=4>[[X]]</font></th><th><font size=4>[[Y]]</font></th><th><font size=4>[[Z]]</font></th> |
| | | | |
| − | * Foi publicado no Diário Oficial da União em 14 de outubro de 2016 a '''Consulta Pública nº 32''', de 11 de outubro de 2016 a respeito da recomendação da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde relativa à proposta de incorporação no SUS do '''certolizumabe pegol para o tratamento da Doença de Crohn'''. Fica estabelecido o prazo de 20 (vinte) dias, a contar da data de publicação desta Consulta Pública, para que sejam apresentadas contribuições devidamente fundamentadas.
| + | </table> |
| − | | |
| − | | |
| − | * Foi publicado no Diário Oficial da União em 14 de outubro de 2016 a '''Consulta Pública nº 33''', de 11 de outubro de 2016 a respeito da recomendação da Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde relativa à proposta de incorporação no SUS do '''citrato de tofacitinibe para o tratamento de pacientes adultos com artrite reumatoide ativa moderada a grave com resposta inadequada a um ou mais Medicamentos Modificadores do Curso da Doença (MMCDs) sintético convencional ou biológico'''. Fica estabelecido o prazo de 20 (vinte) dias, a contar da data de publicação desta Consulta Pública, para que sejam apresentadas contribuições devidamente fundamentadas.
| |
| − | | |
| − | =='''<span style="font-size:large;color:red">''ALERTAS''</span>'''==
| |
| − | | |
| − | | |
| − | '''1. Tobramicina Inalatória
| |
| − | | |
| − | O medicamento [[tobramicina]] '''inalatória''' foi incorporado pelo Ministério da Saúde por meio da [http://conitec.gov.br/images/Relatorios/Portaria/2016/PortariaSCTIE_36_2016.pdf Portaria nº 36, de 26 de outubro de 2016] que torna pública a decisão de incorporar a [[tobramicina]] '''inalatória''' para o tratamento da infecção crônica por Pseudomonas aeruginosa das vias aéreas em pacientes com fibrose cística, conforme Protocolo do Ministério da Saúde, no âmbito do Sistema Único de Saúde - SUS. <span style="font-size:large;color:red">''Para a garantia da disponibilização das tecnologias incorporadas no SUS, conforme determina o artigo 25 do Decreto 7.646/2011, a partir da publicação da decisão de incorporar tecnologia em saúde, as áreas técnicas do Ministério da Saúde terão prazo máximo de 180 dias para efetivar a oferta ao SUS.''</span>
| |
| − | | |
| − | | |
| − | '''2. Protocolo Clínico e Diretrizes Terapêuticas (PCDT) de Imunossupressão no Transplante Hepático em adultos e de Imunossupressão no Transplante Cardíaco
| |
| − | | |
| − | Conforme e-mail recebido pela CONITEC, em 18/10/2016, a SES/SC foi informada que os PCDTs acima passaram por consulta pública nos períodos de 17/08/2016 a 05/09/2016 e 13/09/2016 a 13/10/2016, respectivamente. '''As contribuições encaminhadas encontram-se em análise pelos grupos elaboradores e a expectativa para apreciação do texto final de ambos os protocolos é ainda para o ano de 2016'''. Após a recomendação do texto final pela CONITEC os protocolos seguem para aprovação do Secretário de Ciência e Tecnologia e posteriormente para a publicação, oficializando assim a conduta clínica de imunossupressão para os transplantes hepáticos e cardíacos frente as novas tecnologias incorporadas no SUS. Até o momento o medicamento [[everolimo]] não está disponibilizado para imunossupressão nos transplantes hepáticos em adultos e [[sirolimo]], [[tacrolimo]] e [[everolimo]] não estão disponibilizados para imunossupressão nos transplantes cardíacos, pois aguarda-se esta regulamentação de uso via PCDT. Os PCDTs estão na última etapa de elaboração e consolidação do texto final, portanto próximos da publicação.
| |
| − | | |
| − | | |
| − | '''3. Dolutegravir e Darunavir
| |
| − | | |
| − | Os membros presentes na reunião da CONITEC de 1º de setembro de 2016 deliberaram por unanimidade – [http://conitec.gov.br/images/Relatorios/2016/Relatorio_DolutegravirDarunavir_final.pdf Relatório de Recomendação n° 227] - recomendar a ampliação de uso de [[dolutegravir]] em esquemas de primeira linha e [[darunavir]] em esquemas de segunda linha de terapia no tratamento da infecção pelo HIV.
| |
| − | | |
| − | Os medicamentos [[dolutegravir]] e [[darunavir]] foram incorporados pelo Ministério da Saúde por meio da [http://conitec.gov.br/images/Relatorios/Portaria/2016/PortariaSCTIE_35_2016.pdf Portaria nº 35, de 28 de setembro de 2016] para o tratamento de para o
| |
| − | tratamento da infecção pelo HIV, no âmbito do Sistema Único de Saúde - SUS.<span style="font-size:large;color:red">''Para a garantia da disponibilização das tecnologias incorporadas no SUS, conforme determina o artigo 25 do Decreto 7.646/2011, a partir da publicação da decisão de incorporar tecnologia em saúde, as áreas técnicas do Ministério da Saúde terão prazo máximo de 180 dias para efetivar a oferta ao SUS.''</span>
| |
| − | | |
| − | [http://portalsaude.saude.gov.br/index.php/cidadao/principal/agencia-saude/25857-saude-oferecera-melhor-tratamento-do-mundo-para-hiv-aids Saúde oferecerá melhor tratamento do mundo para HIV/Aids] Acesso em 04/10/2016
| |
| − | | |
| − | | |
| − | '''4. Rivastigmina Adesivo Transdérmico
| |
| − | | |
| − | O medicamento [[rivastigmina]] '''na apresentação adesivo transdérmico''' foi incorporado pelo Ministério da Saúde por meio da [http://conitec.gov.br/images/Relatorios/Portaria/2016/PortariasSCTIE_30a34_2016.pdf Portaria nº 31, de 20 de setembro de 2016] que torna pública a decisão de incorporar a rivastigmina adesivo transdérmico para o tratamento de demência para Doença de Alzheimer, conforme Protocolo Clínico e Diretrizes Terapêuticas do Ministério da Saúde, no âmbito do Sistema Único de Saúde - SUS. <span style="font-size:large;color:red">''Para a garantia da disponibilização das tecnologias incorporadas no SUS, conforme determina o artigo 25 do Decreto 7.646/2011, a partir da publicação da decisão de incorporar tecnologia em saúde, as áreas técnicas do Ministério da Saúde terão prazo máximo de 180 dias para efetivar a oferta ao SUS.''</span>
| |
| − | | |
| − | | |
| − | '''5. AVASTIN® - Bevacizumabe
| |
| − | | |
| − | Por meio da [http://portal.anvisa.gov.br/documents/10181/2971795/RDC_111_2016_.pdf/f12db9d9-fe9a-4ce0-85ea-a2d70226a4aa RDC n° 111, de 6 de setembro de 2016], publicado no Diário Oficial da União – DOU, em 8 de setembro de 2016, foi autorizado uso excepcional, em carácter temporário, no âmbito do Sistema Único de Saúde (SUS), o medicamento Avastin® (25 mg/ml solução para diluição para infusão), da empresa Produtos Roche Químicos e Farmacêuticos, que tem como princípio ativo o fármaco [[bevacizumabe]], no tratamento da Degeneração Macular Relacionada à Idade (DMRI).
| |
| − | | |
| − | Entretanto, algumas questões ainda permanecem sem resposta e precisam ser esclarecidas e regularizadas para que seja iniciado o tratamento de DMRI pelo SUS no Estado de Santa Catarina. Conforme contato com a Diretoria de Assistência Farmacêutica – DIAF/SC em 19/09/2016, a DIAF até o momento não repassou maiores informações pertinentes ao caso, nem tampouco o Ministério da Saúde.
| |
| − | | |
| − | | |
| − | '''6. Oncológicos
| |
| − | | |
| − | Foram atualizados os seguinte medicamentos oncológicos: Abiraterona, Anastrozol, Bevacizumabe, Bicalutamida, Bortezomibe, Brentuximabe, Cabazitaxel, Ciproterona, Crizotinibe, Flutamida, Fulvestranto, Gosserrelina, Ipilimumabe, Irinotecano, Lapatinibe, Leuprorrelina, Mercaptopurina, Panitumumabe, Pazopanibe, Pemetrexede, Pertuzumabe, Ponatinibe, Trastuzumabe entansina, Triptorrelina, Vandetanibe, Vemurafenibe e Vismodegib.
| |
| − | | |
| − | | |
| − | '''7. Foram atualizados os medicamentos que constam na lista da Farmácia Popular, da Deliberação 501/CIB/13, Parte da RENAME e do CEAF.
| |
| − | | |
| − | ==Informações==
| |
| − | | |
| − | - [[Acesso ao Componente Especializado da Assistência Farmacêutica - CEAF]]
| |
| − | | |
| − | - [[Ausência de Registro na ANVISA]]
| |
| − | | |
| − | - [[Comissão Intergestores Bipartite CIB]]
| |
| − | | |
| − | - [[CONITEC]]
| |
| − | | |
| − | - [[Guia Entendendo a Incorporação de Tecnologias em Saúde no SUS – Como se Envolver]] <span style="font-size:large;color:red">''Novo!''</span>
| |
| − | | |
| − | - [[ Endereços/Contatos CACON/UNACONs ]]
| |
| − | | |
| − | - [[ Medicamentos - Conceitos e Informações Técnicas]]
| |
| − | | |
| − | - [[Medicamentos de Combate a AIDS e ao HIV - Antirretrovirais (ARV)]]
| |
| − | | |
| − | - [[Medicamentos Manipulados]]
| |
| − | | |
| − | - [[ Medicamento "off label"]]
| |
| − | | |
| − | - [[ Prescrições Médicas ]]
| |
| − | | |
| − | - [[RENAME]]
| |
| − | | |
| − | - [[Tratamento oncológico no SUS]]
| |
| − | | |
| − | ==Programas==
| |
| − | | |
| − | - [[Programa Estadual de Vigilância e Controle das Hepatites Virais (PEHV)]]
| |
| − | | |
| − | - [[Programa Farmácia Popular do Brasil]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF)]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Hanseníase]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Tracoma]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Tabagismo]]
| |
| − | | |
| − | - [[Componente Estratégico da Assistência Farmacêutica (CESAF) - Tuberculose]]
| |
| − | | |
| − | - [[Componente Especializado da Assistência Farmacêutica (CEAF)]]
| |
| − | | |
| − | ==Legislação==
| |
| − | | |
| − | - [http://bvsms.saude.gov.br/bvs/saudelegis/gm/2013/prt0874_16_05_2013.html Política Nacional para a Prevenção e Controle do Câncer]
| |
| − | | |
| − | ==Links Úteis==
| |
| − | -
| |
| − | [http://portalses.saude.sc.gov.br/index.php?option=com_docman&task=doc_download&gid=7659&Itemid=128 Deliberação 501/CIB/13 de 27 de novembro de 2013]
| |
| − | | |
| − | - [http://cgj.tjsc.jus.br/saude/index.htm Portal Assistência à Saúde], da Corregedoria-Geral da Justiça/SC
| |
| | | | |
| − | - [http://rebrats.saude.gov.br/ Rede Brasileira de Avaliação de Tecnologias em Saúde (REBRATS)]
| + | =='''Medicamentos por CID e PCDT'''== |
| | | | |
| − | - [http://portalsaude.saude.gov.br/index.php?option=com_content&view=article&id=11635&Itemid=702 Componente Especializado da Assistência Farmacêutica] | + | '''Um novo recurso está disponível no site da CONITEC:''' o '''painel interativo de Medicamentos por CID e Protocolos Clínicos e Diretrizes Terapêuticas (PCDT)''' possibilita uma consulta rápida dos medicamentos e dos códigos da Classificação Internacional de Doenças (CID-10) contemplados nas diretrizes do Ministério da Saúde. |
| | | | |
| − | - [http://portalsaude.saude.gov.br/index.php/o-ministerio/principal/leia-mais-o-ministerio/840-sctie-raiz/daf-raiz/cgceaf-raiz/cgceaf/l3-cgceaf/11646-pcdt Protocolos Clínicos E Diretrizes Terapêuticas (PCDT)], do Ministério Da Saúde
| + | '''Obs:''' ''a ferramenta não substitui a leitura integral do documento, uma vez que a indicação de cada medicamento exige atenção a critérios adicionais, como idade do paciente, histórico de tratamentos, estágio da doença, entre outros.'' |
| | | | |
| − | - [http://www.projetodiretrizes.org.br/ Projeto Diretrizes - CFM AMB ANS]
| + | <span style="color:blue">[https://www.gov.br/conitec/pt-br/protocolos-clinicos-e-diretrizes-terapeuticas/medicamentos-por-cid-e-pcdt '''Clique aqui'''] '''para acessar o painel.''' |
| | | | |
| − | - [http://portalsaude.saude.gov.br/index.php/o-ministerio/principal/secretarias/sctie/conitec Comissão Nacional de Incorporação de Tecnologias no SUS (CONITEC)]
| + | =='''Recomendações avaliadas pela CONITEC'''== |
| | | | |
| − | - [http://portalsaude.saude.gov.br/index.php/o-ministerio/principal/leia-mais-o-ministerio/840-sctie-raiz/daf-raiz/cgceaf-raiz/cgceaf/l3-cgceaf/11647-consulta-publica Consultas Públicas De Protocolos Clínicos E Diretrizes Terapêuticas]
| + | *[[Medicamentos incorporados - 2026]] |
| | | | |
| − | - [http://www.ncbi.nlm.nih.gov/pubmed/ PubMed (artigos científicos da área da saúde)] | + | *[[Medicamentos incorporados - 2025]] |
| | | | |
| − | - [http://www.scielo.br/?lng=pt SciELO (biblioteca eletrônica de periódicos científicos brasileiros)] | + | *[[Medicamentos incorporados - 2024]] |
| | | | |
| − | - [http://bvsalud.org/ Biblioteca Virtual em Saúde] | + | *[[Medicamentos incorporados - 2023]] |
| | | | |
| − | - [http://portal2.saude.gov.br/saudelegis/LEG_NORMA_PESQ_CONSULTA.CFM Saúde Legis] | + | *[[Medicamentos incorporados - 2022]] |
| | | | |
| − | - [http://scholar.google.com.br/schhp?sourceid=navclient&ie=UTF-8&hl=pt-BR Google acadêmico]
| + | *[[Medicamentos incorporados - 2021]] |
| | | | |
| − | - [http://www7.anvisa.gov.br/datavisa/Consulta_Produto/consulta_medicamento.asp Consulta de registro do medicamento na ANVISA] | + | *[[Medicamentos incorporados - 2020]] |
| | | | |
| − | ==Residual==
| + | *[[Medicamentos incorporados - 2019]] |
| | | | |
| − | - [[Alergia à proteína do leite de vaca]]
| + | *[[Procedimentos, exames e insumos incorporados - 2026]] |
| | | | |
| − | - Artroplastia de quadril/[[Prótese (de quadril)]]
| + | *[[Procedimentos, exames e insumos incorporados - 2025]] |
| | | | |
| − | - [[Cross-linking]] (cirurgia para ceratocone)
| + | *[[Procedimentos, exames e insumos incorporados - 2024]] |
| | | | |
| − | - [[Curativos]]
| + | *[[Procedimentos, exames e insumos incorporados - 2023]] |
| | | | |
| − | - [[DMRI|Degeneração Macular Relacionada à Idade (DMRI)]]
| + | *[[Procedimentos, exames e insumos incorporados - 2022]] |
| | | | |
| − | - [[Eletroconvulsoterapia]]
| + | *[[Procedimentos, exames e insumos incorporados - 2021]] |
| | | | |
| − | - [[Internação Psiquiátrica Compulsória]]
| + | *[[Procedimentos, exames e insumos incorporados - 2020]] |
| | | | |
| − | - [[Intolerância à lactose]]
| + | *[[Procedimentos, exames e insumos incorporados - 2019]] |
| | | | |
| − | - [[Litíase urinária]] (pedras nos rins, ureteres ou bexiga)
| + | =='''Componentes da Assistência Farmacêutica'''== |
| | | | |
| − | - [[Meia Elástica]]
| + | *[[Componente Básico da Assistência Farmacêutica - CBAF]] |
| | | | |
| − | - [[Método Bobath]]
| + | *[[Componente Especializado da Assistência Farmacêutica - CEAF]] |
| | | | |
| − | - [[Método Pediasuit]] <span style="font-size:large;color:blue">''Em Atualização''</span>
| + | *[[Componente Estratégico da Assistência Farmacêutica - CESAF]] |
| | | | |
| − | - [[Monitorização Neurofisiológica Intraoperatória]]
| + | *[[Tratamento oncológico no SUS|Componente da Assistência Farmacêutica em Oncologia - AF-Onco]] |
| | | | |
| − | - [[Óculos]]
| + | =='''Residual'''== |
| | | | |
| − | - [[Oxigenoterapia Domiciliar]]
| + | *[[Doenças]] |
| | | | |
| − | - [[Oxigenoterapia Hiperbárica]]
| + | *[[Nutrição]] |
| | | | |
| − | - [[Pet-Scan]]
| + | *[[Procedimentos Médicos Terapêuticos]] |
| | | | |
| − | - [[Quimioterapia Intraperitoneal Hipertérmica]] <span style="font-size:large;color:red">''Novo!''</span>
| + | *[[Procedimentos Médicos Diagnósticos|Procedimentos Médicos Diagnósticos - Exames Complementares]] |
| | | | |
| − | - [[Stent Farmacológico]]
| + | *[[Produtos para saúde (insumos)|Produtos para saúde - Insumos]] |
| | | | |
| − | - [[Videoartroscopia]]
| + | *[[Terapias Complementares]] |
| | | | |
| − | ==Colaboradores==
| + | *[[Pedido de internação / asilamento]] |
| | | | |
| − | Contribuíram para atualização do banco de dados do SISCOMAJ:
| + | *[[Prontuário e Documentos Médicos]] |
| | | | |
| − | - Diretoria de Assistência Farmacêutica (DIAF)
| + | *[[Prerrogativas Médicas]] |
| | | | |
| − | - Diretoria de Vigilância Epidemiológica (DIVE) | + | *[[Tratamento Fora do Domicílio - TFD]] |
| | | | |
| − | - Diretoria de Vigilância Sanitária Estadual
| + | *[[Implante Dentário]] |
| | | | |
| − | '''Término da gestão do SISCOMAJ/COMAJ em março/2016'''
| + | * [[Recomendações do COMESC]] |